เมื่อวันที่ 5 กรกฎาคม Novo Nordisk ได้เปิดตัวการทดลองทางคลินิกระยะที่ 3 ของการฉีด CagriSema ในประเทศจีน โดยมีวัตถุประสงค์เพื่อเปรียบเทียบความปลอดภัยและประสิทธิภาพของการฉีด CagriSema กับเซเมกลูไทด์ในผู้ป่วยโรคอ้วนและน้ำหนักเกินในประเทศจีน
การฉีด CagriSema เป็นการบำบัดแบบผสมผสานที่ออกฤทธิ์ยาวนานภายใต้การพัฒนาโดย Novo Nordisk ส่วนประกอบหลักคือ สเมกลูไทด์ตัวรับตัวเร่งปฏิกิริยา GLP-1 (คล้ายกลูคากอน-1) และคากริลินไทด์อะนาล็อกอะไมลินที่ออกฤทธิ์นานการฉีด CagriSema สามารถฉีดเข้าใต้ผิวหนังได้สัปดาห์ละครั้ง
วัตถุประสงค์หลักคือเพื่อเปรียบเทียบ CagriSema (2.4 มก./2.4 มก.) กับเซเมกลูไทด์หรือยาหลอกสัปดาห์ละครั้งใต้ผิวหนังNovo Nordisk ได้ประกาศผลการทดลอง CagriSema ในการรักษาโรคเบาหวานระยะที่ 2 ซึ่งพิสูจน์แล้วว่าฤทธิ์ลดน้ำตาลในเลือดของ CagriSema ดีกว่าผลของเซเมกลูไทด์ และเกือบ 90% ของผู้เข้ารับการทดลองบรรลุเป้าหมาย HbA1c
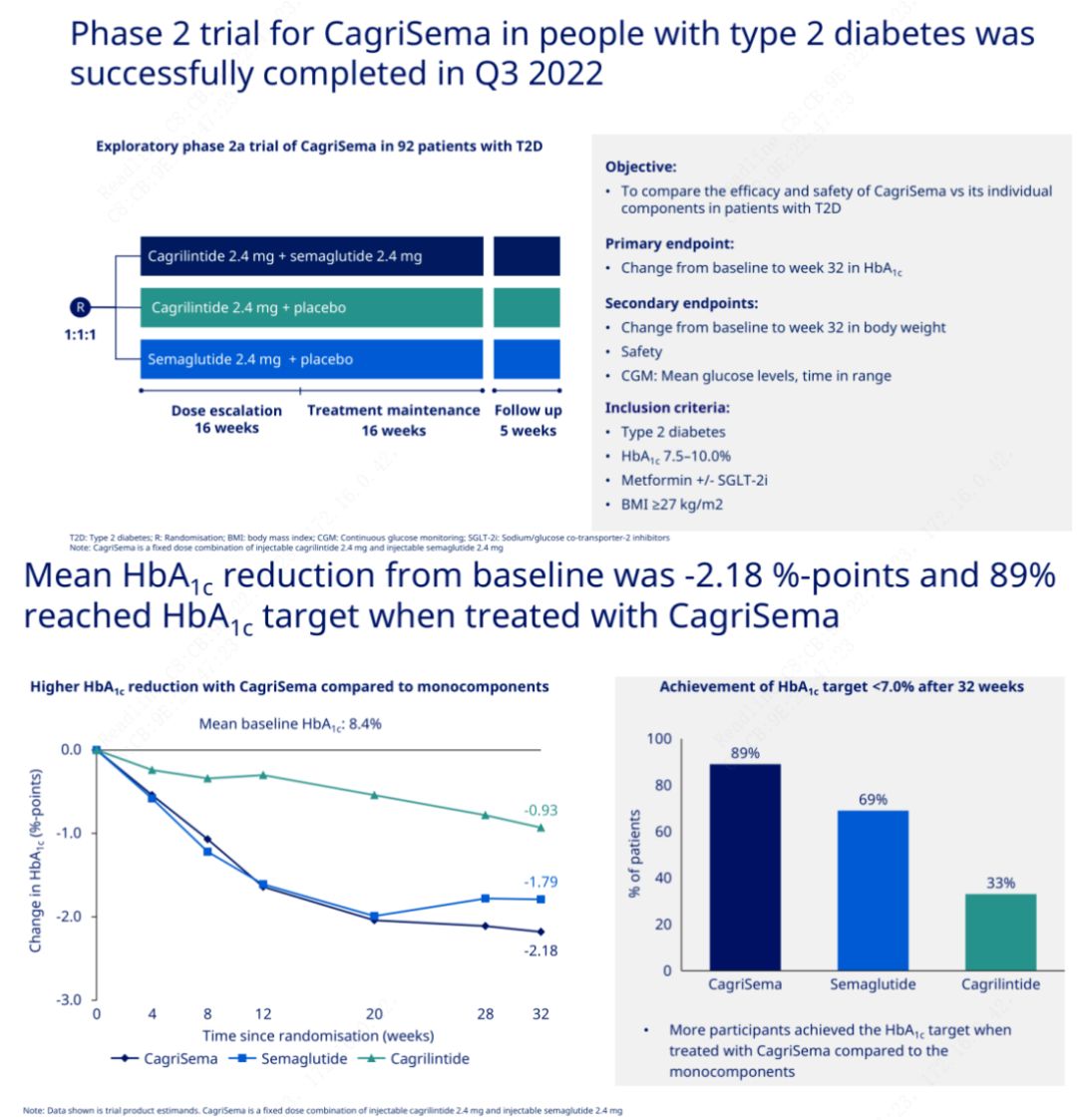
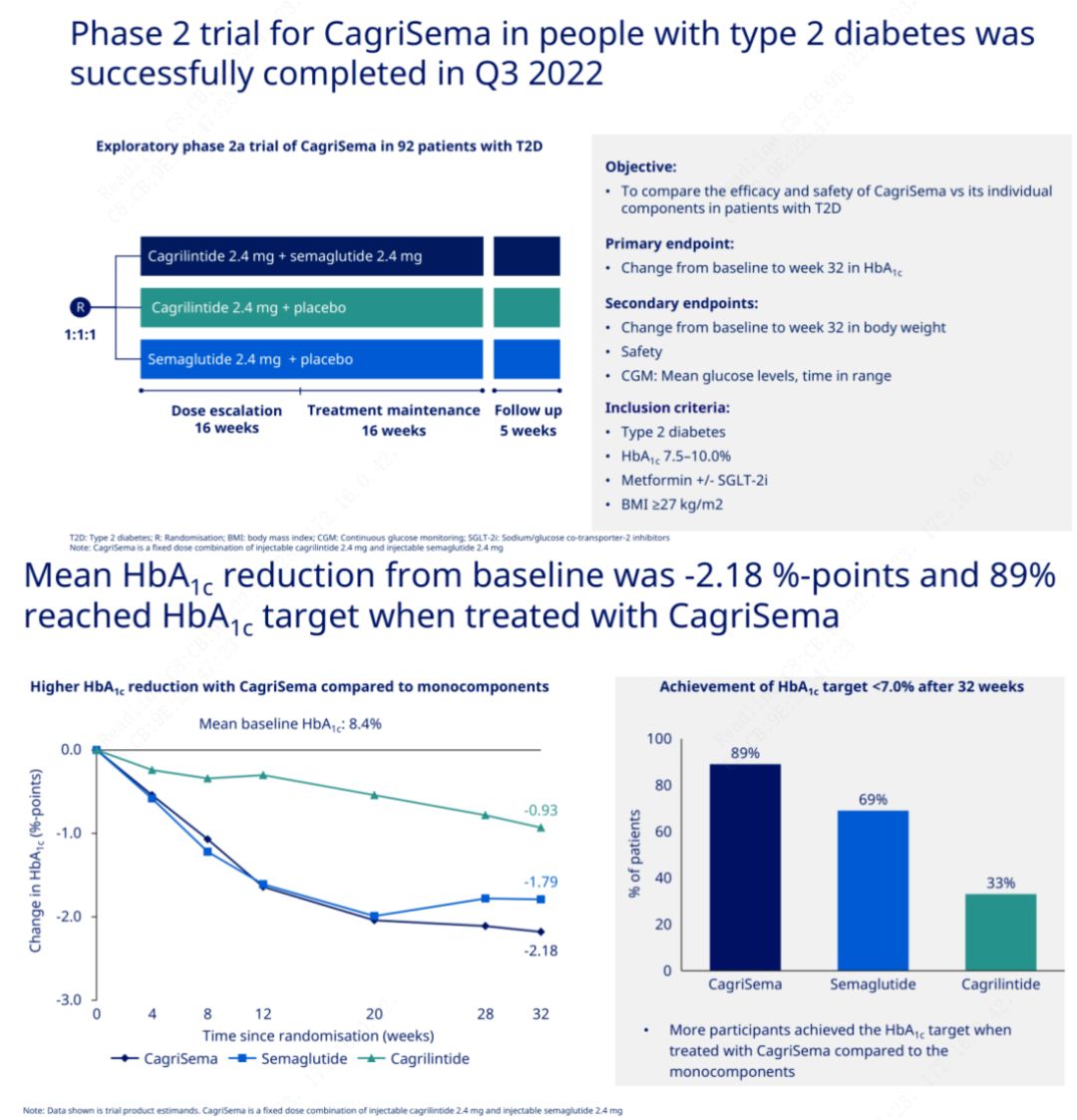
ข้อมูลแสดงให้เห็นว่า นอกเหนือจากผลฤทธิ์ลดน้ำตาลในเลือดที่มีนัยสำคัญ ในแง่ของการลดน้ำหนักแล้ว การฉีด CagriSema ยังมีประสิทธิภาพเหนือกว่าเซเมกลูไทด์ (5.1%) และคากริลินไทด์ (8.1%) อย่างมีนัยสำคัญ โดยลดน้ำหนักได้ 15.6%
ยานวัตกรรม Tirzepatide เป็นตัวเร่งปฏิกิริยาตัวรับ GIP/GLP-1 รายสัปดาห์รายแรกของโลกที่ได้รับการอนุมัติโดยผสมผสานผลของการเพิ่มขึ้น 2 ครั้งเป็นโมเลกุลเดียว โดยฉีดสัปดาห์ละครั้ง และถือเป็นการรักษารูปแบบใหม่สำหรับโรคเบาหวานประเภท 2Tirzepatide ได้รับการอนุมัติจากสำนักงานคณะกรรมการอาหารและยาของสหรัฐอเมริกา (FDA) ในเดือนพฤษภาคม 2565 เพื่อปรับปรุงการควบคุมระดับน้ำตาลในเลือด (ขึ้นอยู่กับอาหารและการออกกำลังกาย) ในผู้ใหญ่ที่เป็นเบาหวานประเภท 2 และปัจจุบันได้รับการอนุมัติในสหภาพยุโรป ญี่ปุ่น และประเทศอื่นๆ
เมื่อวันที่ 5 กรกฎาคม Eli Lilly ได้ประกาศการศึกษาวิจัย SURPASS-CN-MONO ระยะที่ 3 เกี่ยวกับการลงทะเบียนการทดลองทางคลินิกด้านยาและแพลตฟอร์มการเปิดเผยข้อมูลสำหรับการรักษาผู้ป่วยโรคเบาหวานประเภท 2SURPASS-CN-MONO เป็นการศึกษาระยะที่ 3 แบบสุ่ม ปกปิดทั้งสองด้าน มีกลุ่มควบคุมด้วยยาหลอก ซึ่งออกแบบมาเพื่อประเมินประสิทธิภาพและความปลอดภัยของการรักษาด้วยยา tirzepatide เพียงอย่างเดียว เปรียบเทียบกับยาหลอกในผู้ป่วยเบาหวานประเภท 2การศึกษาวางแผนที่จะรวมผู้ป่วย 200 รายที่เป็นโรคเบาหวานประเภท 2 ที่ไม่ได้รับยาต้านเบาหวานใดๆ ใน 90 วันก่อนการนัดตรวจครั้งที่ 1 (ยกเว้นในสถานการณ์ทางคลินิกบางอย่าง เช่น การเจ็บป่วยเฉียบพลัน การเข้ารับการรักษาในโรงพยาบาล หรือการผ่าตัดแบบเลือกได้ในระยะสั้น (≤14 วัน) การใช้อินซูลิน)
โรคเบาหวานประเภท 2 คาดว่าจะได้รับการอนุมัติในปีนี้
เมื่อเดือนที่แล้ว ผลการศึกษาของ SURPASS-AP-Combo ได้รับการตีพิมพ์เมื่อวันที่ 25 พฤษภาคมในวารสาร Nature Medicine ที่โด่งดังผลการศึกษาพบว่า เมื่อเปรียบเทียบกับอินซูลิน กลาร์จิน ยา Tirzepatide มี HbA1c ที่ดีกว่า และน้ำหนักลดลงในประชากรผู้ป่วยเบาหวานชนิดที่ 2 ในภูมิภาคเอเชียแปซิฟิก (จีนเป็นหลัก): HbA1c ลดลงได้ถึง 2.49% และน้ำหนักลดลงได้ถึง 7.2 กิโลกรัม (9.4%) ที่การรักษา 40 สัปดาห์ ไขมันในเลือดและความดันโลหิตดีขึ้นอย่างมีนัยสำคัญ ตลอดจนความปลอดภัยและความทนทานโดยรวมอยู่ในเกณฑ์ดี
การทดลองทางคลินิกระยะที่ 3 ของยา SURPASS-AP-Combo ถือเป็นการศึกษาครั้งแรกของ Tirzepatide ที่ดำเนินการในผู้ป่วยชาวจีนที่เป็นเบาหวานชนิดที่ 2 เป็นหลัก นำโดยศาสตราจารย์จี หลินง แห่งโรงพยาบาลประชาชนมหาวิทยาลัยปักกิ่งSURPASS-AP-Combo สอดคล้องกับผลลัพธ์ของการวิจัยซีรีส์ SURPASS ระดับโลก ซึ่งพิสูจน์เพิ่มเติมว่าพยาธิสรีรวิทยาของโรคเบาหวานในผู้ป่วยชาวจีนมีความสอดคล้องกับของผู้ป่วยทั่วโลก ซึ่งเป็นพื้นฐานสำหรับการวิจัยและพัฒนายาใหม่ไปพร้อมกัน ในประเทศจีนและทั่วโลก และยังให้การสนับสนุนที่มีหลักฐานชัดเจนในการเปิดโอกาสให้ผู้ป่วยชาวจีนได้ใช้ยารักษาโรคเบาหวานตัวล่าสุดและการประยุกต์ใช้ทางคลินิกในประเทศจีนโดยเร็วที่สุด
เวลาโพสต์: Sep-18-2023

